
细胞培养基本设备,基本面和协议

细胞培养基本设备,基本面和协议
完成下面的表格,我们将电子邮件您的PDF版本“细胞培养基本设备,基本面和协议”
新的细胞培养?然后看看。在这里你会发现一切细胞培养的基本概述,建立细胞培养实验室的理解基本原则和基本技巧。一个伟大的起点跳板到细胞生物学的世界。
细胞培养所需的基本设备和试剂
细胞培养实验室设计
细胞培养安全
细胞培养基本知识
——培养条件
——主要与细胞永生化
——附着和悬挂的文化
——哺乳动物和非哺乳类文化
——细胞生长和confluency
——选择一个细胞系
——细胞系验证
——细胞培养媒体:选择正确的媒体为你的细胞
标准的细胞培养协议
——无菌技术
——原代细胞分离
-接种/使细胞
——低温贮藏和解冻
——测试支原体感染的细胞
——细胞计数
——细胞转染
细胞培养是什么?
细胞培养是指去除细胞从动物或植物和后续培养科学研究的人工环境。最早的细胞培养技术是100多年前开发的,从那时起科学取得了巨大的突破。今天,它是一个基本工具在世界各地的实验室用于研究细胞的正常生理和生物化学,机制潜在疾病,包括癌症,和的影响药物和有毒化合物。它也被运用于药物筛选和发展ent和大规模生产的生物化合物,如疫苗和治疗性蛋白质。1,2还有一个越来越重要的角色的细胞培养在食品行业测试污染物而在细胞农业和非养殖肉生产,以减轻环境负担。
细胞培养所需的基本设备和试剂
研究要求细胞培养工作和执行基本的细胞培养协议,有几个关键的设备和一些基本的所需试剂,总结在表1和2。
表1:细胞培养所需的基本设备。3,4,5这些照片是创建BioRender.com。

完全培养基
|
见下面的部分媒体对你的细胞。 |
|
缓冲溶液
|
磷酸盐(PBS)用于洗涤细胞。 |
|
分离剂
|
酶用于分离附着细胞文化培养器皿,如胰蛋白酶。 |
|
冷冻保存剂 |
一个代理,降低媒体的冰点,减缓冷却速率降低冰晶形成的风险可破坏细胞,导致细胞死亡。二甲亚砜(DMSO)是最常用的。 |
同样重要的是访问去离子的蒸馏水和冰。实验的性质会通知执行需要的试剂。
细胞培养实验室设计
有几个重要的设计考虑任何细胞培养所需的设置。最重要的方面是使用设计保持无菌,无菌环境防止污染的细胞。首先,一个独立的封闭的房间或实验室应该使用一个入口/出口点。用肥皂和洗手液洗手水池应靠近手打扫实验室的出入境。专门的细胞培养实验室外套和护目镜应存储实验室门口。层流罩和孵化器应该远离入口降低污染风险。也很重要位置罩和孵化器远离空调,以防止任何可能被污染的气流进入无菌工作环境和孵化器。应该有充足的明确的工作表面,需要定期消毒有足够的存储空间,确保表面依然清晰。所有必要的设备和耗材应该在实验室防止退出和重新访问。层流罩的符合人体工程学的环境是很重要的有足够的房间抽屉或可移动的手推车的耗材手头工作时以及孵化器,显微镜和离心机。6同样重要的是使用适当的塑料耗材可推断出的化合物浸出的风险最小化和污染你的细胞培养。
细胞培养安全
细胞培养实验室提出了风险处理和操纵细胞和组织以及有毒、腐蚀性或诱变溶剂和试剂。因此,坚持标准微生物实践和技术是至关重要的,以减轻风险,确保安全。有四个提升的生物安全防护水平,被称为生物安全级别(声波测井)。每一层都有微生物标准实践,安全设备和设施保障实现在处理危险生物材料和代理。BSL-1是最常见的基本的安全保护研究和临床实验室使用的代理在哪里不清楚导致疾病在正常、健康的人类。BSL-2适合有中等代理不同程度的导致人类疾病通过摄入或经皮或粘膜接触。大多数细胞培养实验室应该至少BSL-2,但确切的需求取决于所使用的生物材料和工作的类型。BSL-3需要代理构成严重的和潜在的致命感染和BSL-4,控制水平最高,需要实验室处理传染性病原体构成高个人威胁生命的疾病的风险。4,7
下面列出基本的细胞培养实验室的安全建议。决不是完整的列表,应该补充适当的生物安全水平的建议。
——总是穿适当的个人防护装备(PPE)包括实验室外套,手套和护目镜。
——总是阅读材料安全数据表(MSDS)任何物质时使用,以确保适当的安全预防措施处理。
-清除所有工作表面之前和之后你的实验。
——常规清洁实验室设备,即使它没有被污染。
-避免气溶胶和/或飞溅的创建。
——洗手后使用有潜在危险的材料和在离开实验室之前。
-清除所有潜在传染性材料前处理。
——报告任何事件可能导致接触传染性材料适当的人员(如实验室主管、安全官)。
——不吃,喝酒、抽烟、处理的隐形眼镜,适用于化妆品、在实验室或储存食物供人类食用。
细胞培养基本知识
培养条件
细胞生存和增殖,至关重要的是,复制的文化环境,尽可能最好的,细胞的生理环境。可以控制培养条件包括温度、相对湿度和有限公司2水平以及与媒体相关的因素,如营养成分、pH值、同渗重摩和补货的数量和频率。这些变量会随着时间波动,所以他们应该监控。表3强调大多数哺乳动物细胞培养的最佳培养条件,但是确实存在异常。5
表3:最佳的细胞培养条件对大多数哺乳动物细胞。1,2,4,8
pH值
|
7.0 - -7.4
|
|
渗透性
|
280 - 320 mOsmol /公斤 |
|
有限公司2
|
5 - 10%
|
|
温度 |
35-37◦C
|
主要与细胞永生化
主细胞培养细胞直接从完整的孤立的组织或器官碎片和生长在一道菜。一旦主文化亚文化圈第一次就称为细胞株。主要细胞系的使用寿命有限,只能他们的亚文化10 - 20倍,才能达到一种衰老状态(停止细胞分裂)。1
一些细胞系没有限制他们的寿命和无限增殖的能力。这些被称为连续或细胞系永生化细胞系。不灭的细胞可以发生在许多方面。癌细胞有固有的突变,使细胞在文化传播没有限制。正常细胞最初有一个有限的寿命可以转换成为无限增殖通过增长促进基因中的突变。正常细胞生长在文化还可以故意不灭的化学治疗或引入tumor-causing病毒激活促生长的基因。图1显示了主要的进化改变连续细胞系和理论从每个阶段细胞产生。9
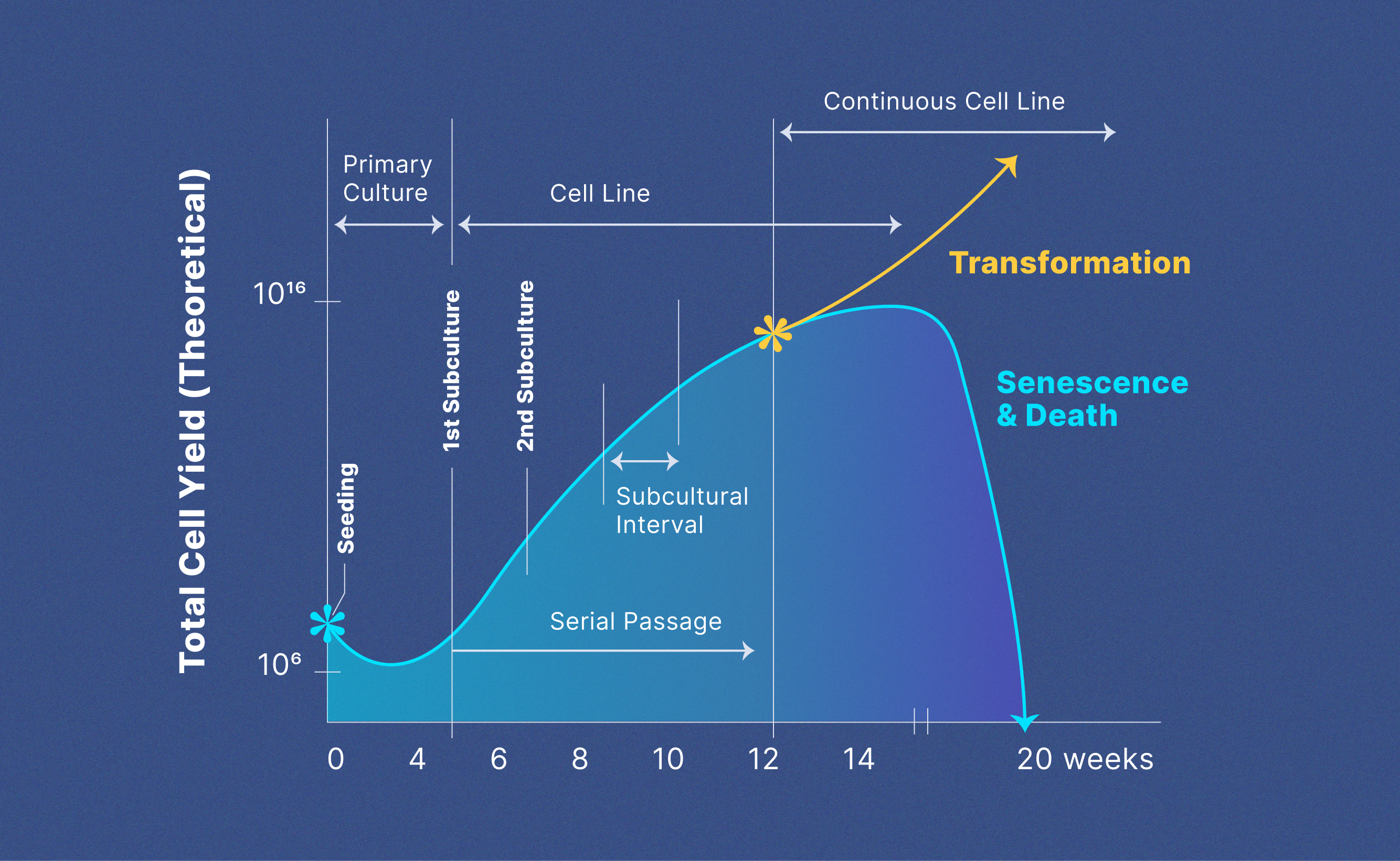
图1: 进化的主要细胞连续细胞系和理论产量。
附着vs悬挂文化
贴壁细胞生长在一个单层细胞培养器皿表面。需要使用通道时,分离剂从表面分离。他们重新接合表面镀上几小时。悬浮细胞不会表面形成单层细胞培养器皿,但仍悬浮。细胞团形式,特别是在高密度。1,10
哺乳动物和非哺乳类文化
哺乳动物细胞培养是最普遍的现象,然而,细胞可以培养大量的生物,如植物、昆虫、细菌和酵母。植物细胞培养通常生长在液体培养基中细胞悬液文化或固体培养基上愈伤组织文化。细胞黑腹果蝇或粘虫Spodoptera frugiperda昆虫细胞系的例子是用于生化检测,或分别表达重组蛋白。细菌和酵母,少量的细胞通常生长在一个坚实的支持,其中包含营养嵌入式,通常凝胶,如琼脂,而大规模的文化才能生长细胞悬浮在营养肉汤。
细胞生长和confluency
细胞培养生长通常发生在四个阶段(图2)。滞后阶段发生在细胞适应文化条件和不分裂。日志阶段发生在细胞分裂正在积极。这是最好的阶段细胞实验和数据收集。细胞应该是他们的亚文化当他们到达日志后期阶段。这发生在过度拥挤。当细胞方法过度拥挤,细胞增长放缓。这被称为固定相或高原期。细胞在此阶段细胞的风险压力。当细胞死亡的自然过程主导,一个细胞群被认为是在死亡阶段,也称为衰落阶段。当细胞计数的日志时间画,它生成一个s形曲线如图2所示。 It is important to note that the amount of time spent in each phase differs between individual cell lines and cultures.11

图2: 细胞生长的四个阶段。
一个重要的指标来描述单层细胞培养是融合。它是培养容器表面积的百分比出现覆盖着一层细胞在显微镜观察到。例如,当表面积的一半由细胞培养容器,融合的人口被认为是50%。图3中的示意图显示了不同的细胞融合的例子。细胞密度是用来描述细胞生长在悬架。2,5

图3: 示意图显示4字段的视图在显微镜下细胞的描述为20%,50%,80%和100%的融合。这张照片是创建BioRender.com。
选择一个细胞系
有成千上万的细胞建立线用于世界各地的实验室,可以从商业或非营利性的供应商购买(细胞银行)。关键是获得从信誉良好的供应商作为细胞细胞系验证和3。从其他实验室获得细胞系有高风险污染和缺乏细胞系验证,因此建议。
表4中的条件时应考虑选择合适的细胞系对于一个实验。细胞系的选择将在很大程度上取决于实验的性质和要求。
物种
|
种特异的细胞线需要使用吗?如果不是这样,人类和non-primate细胞系通常需要减少生物安全限制可能是有利的。 |
|
功能特征
|
使用合适的细胞系实验。例如,肝脏,kidney-derived细胞系可能更适合毒性测试。 |
|
有限或无限增殖
|
有限细胞系更功能有关,因为他们没有经历了不灭,但是永生化细胞系往往易于维护和克隆。 |
|
正常或转换 |
转化细胞系有提高增长率和更高的电镀效率是有利的,但是细胞经历了一个永久的基因变化。这可能影响你的实验吗? |
|
生长条件和特点 |
增长率,克隆效率,或饱和密度很重要对你的实验吗?你需要贴壁细胞还是暂停?举个例子,如果你想表达的重组蛋白高收益你会选择一个快速增长的细胞系能悬浮生长。 |
表5列出了20个常用细胞系及其特征包括物种、组织起源和形态。细胞的形态通常描述为纤维母细胞,上皮细胞或淋巴母细胞表明两种细胞的起源和外表。成纤维细胞是双极或多极和细长的形状;上皮细胞有一个多边形形状和一般表现出更多的常规尺寸和淋巴母细胞细胞表现出球面轮廓,通常生长在悬架。1,5
表5:20个常用细胞系及其特点。
细胞系 |
起源 |
物种 |
形态 |
文化类型 |
子宫颈 |
人类 |
上皮 |
附着 |
|
胚胎肾 转化与 腺病毒 |
人类 |
上皮 |
附着 |
|
外周血 |
人类 |
淋巴母细胞 |
悬架 |
|
人类早幼粒细胞 白血病细胞 |
人类 |
Lymphoblast-like |
悬架 |
|
乳腺癌 |
人类 |
Epithelial-like |
附着 |
|
骨 |
人类 |
上皮 |
附着 |
|
前列腺癌 |
人类 |
上皮 |
附着,可以适应悬挂 |
|
肺癌 |
人类 |
Epithelial-like |
附着 |
|
肝癌 |
人类 |
Epithelial-like |
附着 |
|
骨髓 |
人类 |
上皮 |
附着或暂停 |
|
胚胎干细胞 |
人类 |
淋巴母细胞 |
悬架 |
|
卵巢的中国 |
仓鼠 |
上皮 |
附着 |
|
肾上皮细胞 |
非洲绿猴 |
上皮 |
附着 |
|
肾细胞 |
非洲绿猴 |
纤维母细胞 |
附着 |
|
纤维母细胞 |
鼠标 |
纤维母细胞 |
附着 |
|
纤维母细胞 |
叙利亚仓鼠 |
纤维母细胞 |
附着 |
|
上皮细胞 |
狗 |
上皮 |
附着 |
|
成肌细胞 |
老鼠 |
成肌细胞 |
附着 |
|
胚胎成纤维细胞 细胞 |
斑马鱼 |
纤维母细胞 |
附着 |
|
卵巢 |
降粘虫(Spodoptera frugiperda) |
上皮 |
暂停或附着 |
细胞系验证
细胞培养是一个重要的工具在世界各地的实验室。然而,细胞系可以误诊或与其他细胞污染。这个无效发表的数据和实验室的时间和资源的浪费。由于这个问题的严重性,而需要确保有效和可重复的结果现在期刊、机构及机构建议或要求细胞系验证。细胞系验证可以通过使用多态基因分析短串联重复序列(STR)基因座。细胞应在收到认证一个新的细胞系和定期在他们的亚文化。12
细胞培养基:选择正确的媒体对你的细胞
培养的细胞是美联储液体媒体。有四个关键因素时要考虑组成介质的细胞被详细地记录在表6。媒介的具体细节要求你的细胞可以找到数据表。总是确保检查数据表细节当培养一个新的细胞系培养条件。
基础培养基
|
基础培养基是营养和盐的混合物。有各种配方包括最低基本培养基(MEM),杜尔贝科修改鹰的介质(DMEM)和罗斯威尔公园纪念研究所(RPMI)。他们可以购买在液态或粉状商业来源。 |
|
谷氨酰胺
|
谷氨酰胺是一种必需氨基酸,是细胞生长所必需的。基础培养基与谷氨酰胺可以购买,如果没有谷氨酰胺,或与一个稳定的二肽谷氨酰胺替代。重要的是要确保你的文化在正常生长条件下谷氨酰胺。 |
|
动物血清 |
细胞通常生长在基础培养基补充动物血清。这就称为“完整”的媒介。血清为细胞提供生长因子和营养需要。胎牛血清(胎牛)是最常用的。在大多数情况下,血清添加这最后一卷在完全培养基混合物在5%和20%之间。 |
|
抗生素 |
细胞培养基通常是补充与抗生素青霉素和链霉素的组合措施,防止细菌生长。与无菌技术,可以增加健康的细胞培养不使用抗生素。 |
标准的细胞培养协议
有几个基本的细胞培养协议执行在所有细胞培养实验室。重要的是要熟悉和了解这些协议。
无菌技术
无菌技术持续练习,可以帮助确保所有文化媒体和文化的不育性血管,从而减少细胞接触的机会污染物可行的,保持文化健康和纯洁。挑剔的无菌技术是一个重要的细胞培养成功阻止文化自由的先决条件微生物污染和细胞交叉污染。无菌技术覆盖处理,试剂和工作总结在表7所示。15,16
表7:总结所需的无菌技术在处理细胞培养。
处理 |
试剂/媒体
|
工作场所
|
·温柔和细心处理。
·灭菌前的所有项目开始。
·无菌吸量管,吸管plasticware和技巧。
·没有接触无菌物品non-sterilized表面(包括手套到您自己的皮肤,衣服或头发)。 |
·Pre-sterilization所有试剂和设备。
·没有可见的污染试剂。
·整除试剂成小卷从防止污染整个股票的工作。
·拥有自己的股票工作消除污染的风险从共享股票。 |
·检查文化罩工作正常。
·工作区域总是无菌整齐。
·经常清洗和de-contamination罩、孵化器和冰箱。 |
原代细胞分离
原代细胞分离可以执行各种复杂的生物样品包括组织(皮肤、肝脏肿瘤、脑、肺等),骨髓、血液、脾和淋巴结。有许多不同的方式为最佳准备样品细胞隔离。所选择的方法取决于你开始样品,可能需要删除某些元素或简单地创建一个单细胞悬液。当孤立细胞从完整的组织,你必须首先破坏细胞外基质的细胞一起使用机械力和/或蛋白水解酶(表8)。 17
原电池的基本轮廓隔离需要单独的部分组织碎或切成2 - 4毫米块无菌剪刀或手术刀。组织块被添加到一个适当的缓冲或平衡盐溶液在冰和洗2 - 3次。游离酶添加根据协议和孵化。细胞被轻轻移液分散。细胞悬液过滤是一个细孔,洗2 - 3次。细胞resuspended介质和播种。18
表8:常用的酶在细胞组织分离协议隔离。18
胶原酶
|
水解胶原蛋白和广泛用于隔离从动物组织细胞。 |
|
透明质酸酶
|
结合使用胶原酶和催化水解的4-β-D-glycosidic联系。 |
|
DNase
|
添加到细胞悬浊液最小化由于DNA受损细胞释放的细胞聚集。 |
|
弹性蛋白酶
|
用于消化组织含有大量的弹性蛋白。 |
|
胰蛋白酶
|
一个丝氨酸蛋白酶特异性肽债券,通常结合其他酶(如弹性蛋白酶和胶原酶)的组织分离。 |
接种/使细胞
接种或者使指的是稀释的细胞已经达到高度融合,使连续的文化传播。贴壁细胞应该通过80 - 90%时支流和悬挂文化时应通过细胞开始丛和文化变得多云。重要的是记录的数量为每个细胞株细胞通道。这有助于监测的可行性和计划实验主要细胞衰老之前到达。它有助于监控无限增殖细胞的年龄越高通道数,进一步遗传漂变。实验不应该执行细胞系 非常高的通道数 。 4
轻轻是很重要的工作活力和细胞倍或严厉的处理会导致细胞损伤或死亡。从来没有吸管中或直接冲洗缓冲到细胞,总是把它轻轻地船的一侧,以避免伤害细胞。当resuspending颗粒或磨碎混合细胞,温和地这样做。
简而言之,贴壁细胞的接种协议如下:媒体删除和细胞与PBS洗一次。分离剂添加,如胰蛋白酶(分解蛋白质,使细胞坚持船)和细胞孵化37°C,直到他们完全分离。超然可以1分钟根据细胞系。监测细胞在显微镜下决定脱离发生时。灭活的胰蛋白酶完全培养基添加到细胞(胰蛋白酶血清灭活,因为它含有蛋白酶抑制剂)和自旋离心机(3 - 5分钟,150 - 300 x g)颗粒细胞。删除媒体(液体的颗粒),轻轻resuspend细胞在新媒体和新培养容器板细胞所需的密度。对于悬浮细胞,不需要胰蛋白酶。细胞收集和离心机(3 - 5分钟,150 - 300 x g)形成一个小球,媒体被移除和细胞在PBS resuspended清洗步骤。缓冲区删除另一轮的离心后,细胞在新媒体和山肩resuspended所需的密度。5
低温贮藏和解冻
细胞系是宝贵的资源,所以至关重要,股市是长期存储保存。低温贮藏指的是冷却和储存的过程中细胞在非常低的温度来维持他们的生存能力。细胞是适合长期储存在温度低于-130°C。
最好的方法同行培养细胞在完全培养基是储存在液氮冷冻保存剂的存在如DMSO溶液。防冷冻的代理降低冰点的媒介,也允许较慢的冷却速度,大大减少冰晶形成的风险可破坏细胞,导致细胞死亡。细胞应该在高浓度冷冻保存(例如,汇合的90%)和最早通过号码。短暂,低温贮藏包括洗涤和粒化细胞,resuspending在完全培养基和DMSO(例如,5% DMSO)和传输1毫升无菌cryovials细胞悬液的解决方案。cryovials放置在受控率cryo-freezer或cryo-freezing容器慢慢细胞必须被冻结。cryo-freezing容器存储在-50到-80°C 24小时然后cryovials转移到液氮存储。2,8
确切的冻结条件取决于使用的细胞系。是非常重要的检查细胞line-specific条件否则你冻结的股票将不会产生可行的细胞解冻时,re-cultured。
来恢复细胞系从液氮存储、冻结在便携式液氮瓶运输容器或干冰细胞培养区域。的DMSO cryovials是有毒的细胞一旦解冻,所以确保高细胞生存能力,细胞必须迅速解冻37°C水浴并立即与预热媒体转移到培养皿。媒体稀释DMSO所以它不再是一种有毒的浓度。一旦解冻细胞传播,通过两次,他们可以被用于实验。是一种很好的做法尽快冻结更多的细胞和替换的瓶从长期储存。2
测试支原体感染细胞
在细胞培养中是一个严重问题支原体感染。这种细菌感染可以改变细胞的行为和新陈代谢,对细胞有不利影响。是非常重要的执行定期支原体检测化验,尤其是对一个连续细胞系。好的做法是为支原体测试时收到一个新的细胞系,股票是解冻和培养,在冻结下来每4- - - - - -6周细胞股市文化。检测支原体是一种简单、可靠的方法染色的细胞样本与赫斯特33258年,特别结合DNA的荧光染料,荧光显微镜下和视图。Mycoplasma-free细胞显示清晰和干净的核赫斯特染色,而mycoplasma-infected细胞也显示模式的丝状染色细胞核外的细菌DNA(图4)。5,19,20.
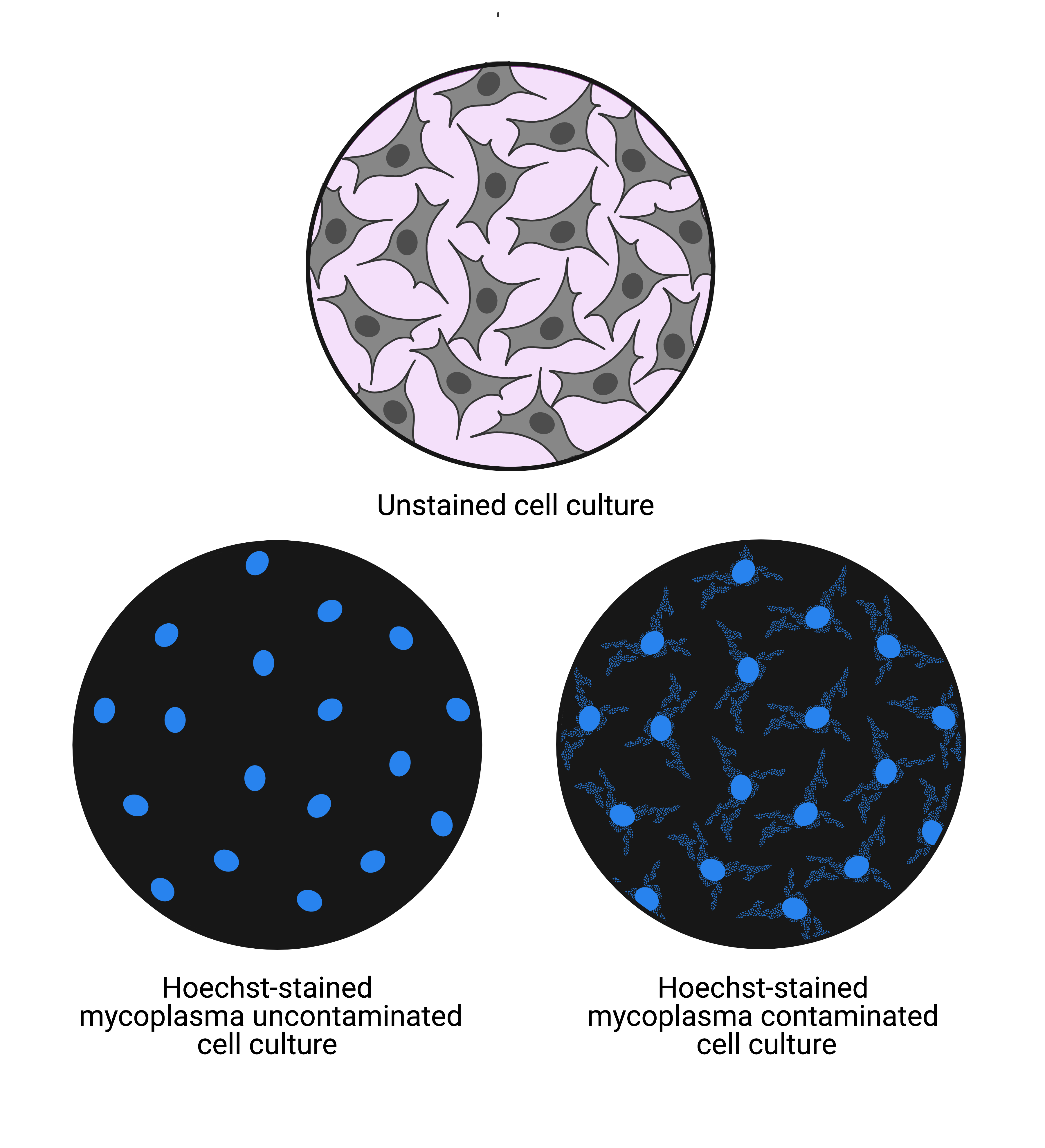
图4: 无污点的示意图显示字段的视图(顶部)细胞和细胞染色与赫斯特33258年支原体未被污染的(左下)和支原体污染(右下角)。未被污染的细胞培养显示细胞核染色污染细胞培养显示细胞核染色和胞质染色。胞质染色表明支原体细菌的DNA的存在。 5 这张照片是创建BioRender.com。
细胞计数
尽管最近开发的自动化细胞计数器,人工细胞计数使用血细胞计数器仍是最常用的方法。血细胞计数器由厚、玻璃显微镜幻灯片有两个网格蚀刻垂直的直线形成腔。一层薄薄的盖玻片也提供。总是在使用前清洁血细胞计数器和盖玻片和位置的盖玻片。加10- - - - - -20μl细胞悬液的两院显微镜幻灯片上盖玻片。使用一个倒置相差显微镜在20 x放大计算细胞的四个外广场如图5所示。你应该是100年计算- - - - - -200个细胞每平方了准确的结果。如果你有太少的细胞,那么下次resuspend你的细胞在媒体。如果你有太多的细胞计数,然后resuspend细胞更高容量的媒体。一旦计算每一个角落,把的数量加起来,除以4。你的细胞浓度将计算x 104细胞/毫升。计算出总细胞,将细胞悬液的浓度。例如,5毫升的浓度的细胞悬液80 x 104细胞/毫升400 x 104细胞或4 x 106细胞或400万细胞。4,5,21,22

图5: 计数细胞血细胞计数器。前面板显示了一个天线和侧视图血细胞计数器的原理图。左下方面板显示在显微镜下计数室的样子。红框突出象限计算。右面板底部的一个例子是计算细胞在一个象限。
细胞转染
转染的细胞是指交付核酸(DNA或RNA)培养细胞。最常用的试剂是阳离子脂质,可以联想到核酸形成带正电的复合物,并允许DNA / RNA相互作用与带负电荷的细胞膜。这导致了有效的输入核酸通过内吞作用进入细胞。这通常被称为脂质转染或脂质转染。此外,核酸可以被交付到细胞电穿孔,共同沉淀DNA的磷酸氢钙,或聚凝胺/ DMSO冲击。交付的DNA通常不会整合在宿主基因组,因此瞬态。实现稳定的基因表达式或击倒,稳定细胞株可以工程化。这需要DNA向量设计和抗生素的选择细胞DNA稳定整合到基因组的位置。23,24
脂质转染转染协议非常简单。从本质上讲,一个解决方案包含正确的浓度DNA / RNA转染是准备和解决方案包含脂质转染试剂的准备。两种溶液混合在一起,培养一段时间根据协议。然后添加到解决方案60- - - - - -80%汇合的细胞和实验可以执行早在转染后6小时。瞬时转染通常持续时间长达72小时。25
引用
1。时答:动物组织文化:原理及应用。动物生物技术:模型发现和翻译。爱思唯尔有限公司;2013:211 - 231。doi: 10.1016 / b978 - 0 - 12 - 416002 - 6.00012 - 2
2。戴维斯、约翰·M。动物细胞培养:基本方法。约翰威利& Sons有限公司;2011年。https://www.wiley.com/en-us/Animal % 3 +电池+文化+基本+方法——p - 9780470666586
3所示。克拉克年代,狄龙j .细胞培养实验室。动物细胞培养:基本方法。约翰•威利父子;2011:1-31。ch1 doi: 10.1002/9780470669815.
4所示。Sandell L,酒井法子d .哺乳动物细胞培养。咕咕叫Protoc Essent实验室技术。5 (1):4.3.1-4.3.32。2011;et0403s5 doi: 10.1002/9780470089941.
5。写明ATCC。动物细胞培养的向导。2021年出版。https://www.atcc.org/ /媒体/ pdf /文化指南/ AnimCellCulture_Guide.ashx
6。莫里斯CB。细胞和组织培养实验室的规划和设计。安全在细胞和组织培养。施普林格荷兰;1998:87 - 101。doi: 10.1007 / 978 - 94 - 011 - 4916 - 7 - _5
7所示。赫尔曼·P, Pauwels k .生物安全动物细胞培养的处理建议。施普林格;2015:689 - 716。doi: 10.1007 / 978 - 3 - 319 - 10320 - 4 - _22
8。华纳博士,酒井法子D, Sandell噢。哺乳动物细胞培养。咕咕叫Protoc Essent实验室技术。2015;10 (1):4.3.1-4.3.33。et0403s10 doi: 10.1002/9780470089941.
9。斯泰西G,麦克唐纳c不灭的主要细胞。细胞培养体外毒理学的方法。施普林格荷兰;2001:27-42。doi: 10.1007 / 978 - 94 - 017 - 0996 - 5 - _3
10。莫顿噢。细胞培养的发展:锚地依赖。费罗斯反式R Soc B Sci杂志。2015,370 (1661):20140040。doi: 10.1098 / rstb.2014.0040
11。Oyeleye OO, Ogundeji圣、Ola SI Omitogun噩。动物细胞培养的基础:现代科学的基础。Biotechnol杂志牧师。2016;11 (2):-。doi: 10.5897 / bmbr2016.0261
12。马克思诉细胞系验证启发。Nat方法。2014;11 (5):483 - 488。doi: 10.1038 / nmeth.2932
13。姚明T, Asayama y .动物细胞培养基:历史、特点、和当前的问题。天线转换开关医学杂志。2017年,16 (2):99 - 117。doi: 10.1002 / 2.12024元人民币
14。PJ价格。哺乳动物细胞的媒体选择的最佳实践。Vitr细胞Dev杂志——动物。2017;53 (8):673 - 681。doi: 10.1007 / s11626 - 017 - 0186 - 6
15。Cote RJ。细胞培养的无菌技术。Protoc细胞生物学观点》。1998;21 (1):1.3.1-1.3.10。cb0103s00 doi: 10.1002/0471143030.
16。戴维斯JM, KL。在细胞培养无菌技术。工业生物技术百科全书。约翰威利& Sons, Inc .);2009:1-20。eib059 doi: 10.1002/9780470054581.
17所示。帕蒂尔R,羽衣甘蓝,鬃毛D,帕蒂尔D隔离,文化和特性的主要人类颊粘膜成纤维细胞的细胞系:外植体enzamytic技术的结合。中华病理学临床口腔医学。2020;24 (1):68 - 75。doi: 10.4103 / jomfp.JOMFP_282_19
18岁。Freshney RI。主要的文化。动物细胞的文化。约翰威利& Sons, Inc .);2005年。cac012 doi: 10.1002/0471747599.
19所示。年轻L,唱J,小主人。检测支原体的细胞培养。Nat Protoc。2010;5 (5):929 - 934。doi: 10.1038 / nprot.2010.43
20.陈TR。原位检测支原体污染的细胞培养的荧光赫斯特33258年污渍。实验细胞Res。1977,104 (2):255 - 262。0014 - 4827 . doi: 10.1016 / (77) 90089 - 1
21。Cadena-Herrera D, Esparza-De劳拉我Ramirez-Ibanez ND, et al .验证三个活细胞计数方法:手动、半自动和自动。Biotechnol报告。2015;7:9-16。doi: 10.1016 / j.btre.2015.04.004
22。湾m .血细胞计数器计数。组织培养。爱思唯尔;1973:395 - 397。doi: 10.1016 / b978 - 0 - 12 - 427150 - 0.50098 x
23。Kim TK Eberwine JH。哺乳动物细胞转染:现在和未来。肛门Bioanal化学。2010,397 (8):3173 - 3178。doi: 10.1007 / s00216 - 010 - 3821 - 6
24。阿赞T, Domb a基因转染的当前发展代理。咕咕叫药物Deliv。2005;1 (2):165 - 193。doi: 10.2174 / 1567201043479902
25。Kumar P,纳,Uchil PD。脂质转染。冷泉Harb Protoc。2019,2019 (3):184 - 187。doi: 10.1101 / pdb.top096248




